Una panoramica del secondo incontro FAD HEpaticLab
Il secondo incontro del ciclo FAD ECM HEpaticLab Approccio sistematico all’encefalopatia epatica (EE): oltre la variabilità clinica, realizzato con il contributo non condizionato di Alfasigma, è andato in onda lo scorso 9 giugno.
Il corso, che fa parte di un percorso di formazione articolato in tre talk show in modalità live che complessivamente forniranno 36 crediti ECM, attivo in modalità asincrona fino al 31 dicembre 2025, ha come obiettivo di promuovere una discussione articolata sul riconoscimento precoce della EE: dai criteri diagnostici differenziali al management clinico.
In questo corso i Relatori sono:
Vincenza Calvaruso Professore Associato di Gastroenterologia, Dipartimento di Promozione della Salute, Materno Infantile, Medicina Interna e Specialistica di Eccellenza “G. D’Alessandro” (PROMISE), Università degli Studi di Palermo.
Paolo Caraceni Professore Ordinario di Medicina Interna, Dipartimento di Scienze Mediche e Chirurgiche, Alma Mater Studiorum Università di Bologna.
Stefano Fagiuoli Professore Ordinario di Gastroenterologia, Dipartimento di Medicina e Chirurgia, Università degli Studi di Milano Bicocca.
Giacomo Germani Professore Associato di Gastroenterologia, Dipartimento di Scienze Chirurgiche Oncologiche e Gastroenterologiche – DiSCOG, Università degli Studi di Padova.
Lorenzo Ridola Professore Associato di Gastroenterologia, Dipartimento di Scienze e Biotecnologie Medico-Chirurgiche, "Sapienza" Università di Roma
Paolo Caraceni - Storia naturale e traiettorie cliniche del paziente con cirrosi scompensata
Nella storia della malattia epatica si è cresciuti pensando alla divisione in 3 fasi che possono durare anni o addirittura decenni, indipendentemente dalla eziologia.
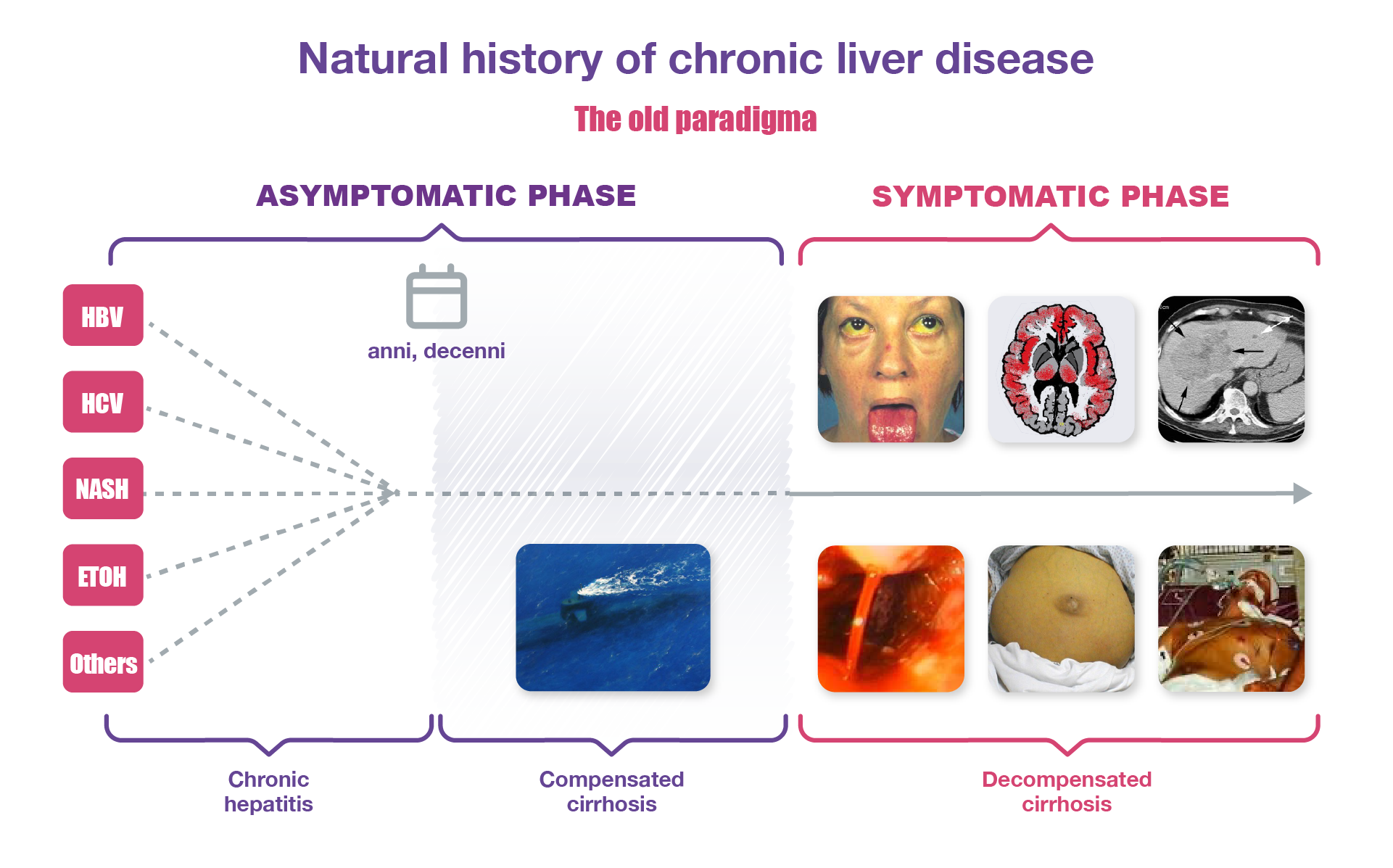
Poi all’improvviso la malattia cambia con l’instaurarsi di manifestazioni severe, anche mortali, e diventa cirrosi scompensata. Negli ultimi 10-15 anni l’eziologia è profondamente cambiata con una netta riduzione delle forme virali grazie ai nuovi farmaci e con l’aumento di forme correlate all’obesità e alla sindrome metabolica e all’alcool. Quindi in un paziente con cirrosi scompensata spesso non è più la manifestazione epatica a dominare ma sono le varie comorbidità, come gli aspetti neurologici che comprendono non solo la EE, ma anche manifestazioni legate a demenza vascolare, all’utilizzo dell’alcool, all’aging. E questo vale anche per le manifestazioni cliniche a carico del cuore, rene e altri organi. Inoltre, sono aumentati gli aspetti psico-sociali che comportano una gestione complessa e una minor aderenza alla terapia.
Per quanto riguarda invece la cirrosi compensata l’elemento dominante è la progressione dell’ipertensione portale. Circa il 5% dei pazienti con cirrosi compensata presenta ogni anno un evento di scompenso, come l’ascite, il sanguinamento e la EE. Il verificarsi di un evento di scompenso peggiora significativamente la prognosi della malattia con la riduzione della sopravvivenza a lungo termine. L’outcome dipende molto dal tipo, dal numero degli eventi di scompenso e dalla loro sequenza cronologica. Lo scompenso acuto (AD) che richiede l’ospedalizzazione, include:
- ascite
- sanguinamento
- EE
- infezione batterica
- combinazione degli eventi
Gli AD sviluppano un quadro di insufficienza epatica acuta su cronica (ACLF) nel 30% dei casi e sono gravati da un’alta mortalità. Il restante 70% che non sviluppa ACLF durante il ricovero va incontro a diversi esiti nei mesi successivi. I pazienti non si scompensano solo acutamente ma possono avere uno scompenso non acuto che non richiede ospedalizzazione ed ha una prognosi migliore. Nel 2022 il Consorzio di Baveno ha introdotto il concetto di paziente ricompensato quando ha eliminato la causa della malattia, non presenta elementi di scompenso, senza trattamento specifico per 12 mesi con miglioramento stabile della funzione epatica.
Lorenzo Ridola - Diagnosi differenziale e fattori scatenanti per la diagnosi dell’Encefalopatia Epatica
Il Dottore comincia con un inquadramento dell’EE: una disfunzione cerebrale secondaria all’insufficienza epatica e/o alla presenza di shunt, che causa uno spettro di segni e sintomi e che spazia da forme non evidenti dal punto di vista clinico al coma. Nell’inquadramento di un paziente cirrotico con un’alterazione dello stato di coscienza è necessaria una profonda diagnosi differenziale con altre malattie.

I fattori di rischio per la EE includono, tra le altre cause:
- la disbiosi
- lo stato infiammatorio sistemico
- lo stress infiammatorio
- le alterazioni del metabolismo del glucosio
- la disfunzione micondriale
- presenza di shunt portosistemici spontanei o iatrogeni
- le alterazioni muscolari
- alcuni farmaci
- l’ammoniaca
I soggetti più vulnerabili sono quelli con malattia epatica avanzata, pregressi episodi di encefalopatia (anche subclinica o minima), presenza di shunt spontanei, alterazioni muscolari (es. sarcopenia) e quelli esposti a farmaci sedativi. L’EE di tipo C si presenta in tre forme: precipitata, spontanea e ricorrente. La forma precipitata si sviluppa in un breve arco di tempo e riconosce spesso uno o più fattori scatenanti, che possono anche coesistere. È quindi fondamentale identificare e correggere questi fattori per risolvere l’episodio encefalopatico. Tra i precipitanti più frequenti vi sono la disidratazione, la costipazione, le infezioni, le alterazioni idro-elettrolitiche, l’emorragia gastrointestinale e l’uso di farmaci ad azione sul sistema nervoso centrale (soprattutto benzodiazepine). Questi eventi si riscontrano sia nei pazienti ambulatoriali sia nei pazienti a domicilio. Nel caso in cui un paziente si presenti con alterazione dello stato mentale, il primo passo è escludere altre cause (infezioni, cause neurologiche, tossiche, ecc.) e cercare, se possibile, informazioni anamnesticamente rilevanti dal caregiver, inclusa l’assunzione recente di sedativi. In particolare, bisogna considerare che alcuni farmaci possono essere stati somministrati per controllare comportamenti disturbanti legati all’EE stessa, innescando un circolo vizioso. È stato sottolineato il ruolo del medico di medicina generale (MMG) come primo punto di contatto, e l’importanza che possa contribuire a un primo inquadramento clinico, utile per accelerare la gestione specialistica.
Il MMG potrebbe rilevare variazioni dell’alvo (es. stipsi), infezioni intercorrenti o modifiche della terapia che costituiscono segnali d’allarme. Infine, è stato ribadito il valore dell’approccio integrato nella valutazione e nella gestione dell’encefalopatia epatica.
Vincenza Calvaruso - Linee Guida, scale di riferimento e criteri classificativi multidimensionali nell’assesment della EE
Le linee guida (LG) sono fondamentali per identificare e e trattare i pazienti nella stessa maniera oltreché per comunicare con la stessa terminologia. Le linee guida dell’American Association for the Study of Liver Diseases ed European Association (Vilstrup et al. Hepatology, 2014) hanno rappresentato un punto di svolta nella classificazione dell’EE sottolineando la necessità di una definizione accurata utile sia alla gestione clinica che alla comunicazione tra specialisti. La definizione di EE poi è stata riportata nelle LG successive, quelle europee del 2022 e quella italiana del 2019. Nelle LG è stato formalizzato pe la prima volta la nomenclatura dell’encefalopatia minima (oggi definita covert encepalopaty), caratterizzata dall’assenza di segni neurologici e dalla normalità dei testi neuropsicologici, che potenzialmente può evolvere verso l’EE manifesta.
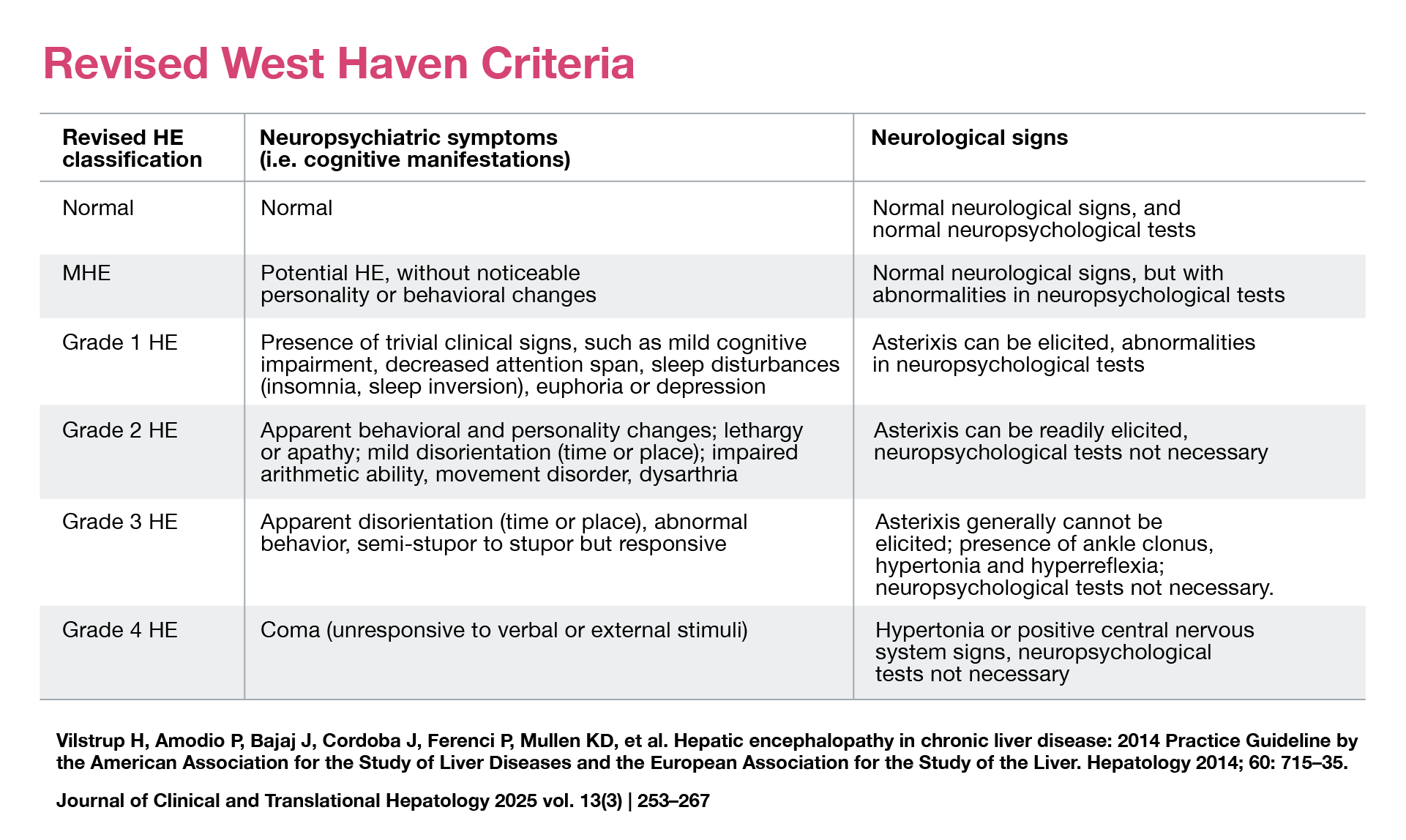
La classificazione distingue l’EE in base al timing di presentazione: forma minima, forme episodiche (almeno 6 episodi di EE nell’arco di sei mesi), ricorrenti e persistenti (con sintomi sempre presenti ed evidenti), oltre che secondo l’eziologia (tipi A, B e C – quest’ultima associata alla cirrosi). La classificazione multiparametrica (Montagnese et al. Dig Liv Dis) del 2019 riprende alcuni dei concetti della LG del 2014 e identifica 4 assi della definizione dell’EE: la tipologia (A B C, quella legata alla cirrosi) a cui viene aggiunta anche la D (acute on chronic liver failure), la severità, la dinamica temporale degli episodi, l’identificazione dei fattori precipitanti e i trattamenti che possono ridurre i livelli di ammonemia. Tra le novità delle linee guida EASL (European Association for the Study of the Liver) pubblicate su Journal of Hepatology 2022, rispetto alle precedenti, sono importanti:
- Il riconoscimento della encefalopatia minima (che raggruppa la minimal e il grado 1), come fattore di rischio indipendente per evento di EE manifesta.
- La raccomandazione di effettuare lo screening soprattutto nei pazienti in contesti selezionati: pazienti con attività lavorativa o che guidano.
- L’utilizzo crescente di score validati come test digitali e strumenti automatizzati per la diagnosi.
- L’indicazione a considerare trattamenti precoci con lattulosio o rifaximina anche nei pazienti con forme minime.
Stefano Fagiuoli - Encefalopatia, TIPS e trapianto di fegato: incroci obbligati?
La TIPS (Transjugular Intrahepatic Portosystemic Shunt) è la creazione di uno shunt artificiale comunicazione artificiale tra il sistema portale e quello venoso sistemico, al fine di ridurre l’ipertensione portale. Tuttavia, saltando il primo filtro epatico, non permettendo la detossificazione, la TIPS favorisce il passaggio sistemico di neurotossine come l’ammoniaca, contribuendo allo sviluppo di encefalopatia epatica post-TIPS (EE post-TIPS).
Fattori predisponenti
- Età >65 anni.
- Livello della malattia sottostante: funzione epatica compromessa (Child-Pugh alto, MELD elevato, ipoalbuminemia, iponatriemia, creatinina elevata)
- Storia pregressa di EE
- Sarcopenia
- Shunt spontanei preesistenti o eccessivo effetto dello shunt
- Farmaci (sedativi, benzodiazepine, ecc.)
Controindicazioni
- Pazienti con malattia cardiaca al limite dello scompenso o scompensata > l’aumento della quota di sangue che dal fegato va al cuore implica che il cuore deve essere ricettivo per il sovraccarico di volume.
- Pazienti con ipertensione polmonare sempre per la modificazione emodinamica
- Pazienti con sepsi severa o non controllabile
Complicanze
- Correlate alla tecnica/posizionamento dello stent come, per esempio, la puntura dell’arteria carotide, episodi di aritmia cardiaca, creazione di fistole epatobiliari
- Correlate alla creazione dello shunt come l’EE (post-TIPS EE) nel 30-50% dei casi, entro un anno dalla TIPS; l’encefalopatia di nuova insorgenza colpisce ~35% dei pazienti; quella refrattaria fino all’8%, può manifestarsi entro un giorno o fino a 210 giorni dalla procedura. La maggior parte dei casi è lieve/moderata e gestibile farmacologicamente.
Prevenzione della post-TIPS EE
- Ottimizzazione del diametro dello stent
- Regolazione del gradiente pressorio portale post-TIPS
- Chiusura di shunt spontanei persistenti (SPSS)
- Non esiste una profilassi farmacologica primaria efficace; la prevenzione secondaria segue le LG per la gestione generale della EE, con uso combinato di lattulosio e rifaximina
Trattamento
- L’EE post-TIPS si gestisce come le forme senza TIPS: lattulosio e rifaximina sono cardini di terapia
- Nei casi refrattari: riduzione o chiusura dello shunt; in pazienti candidabili, trapianto epatico come trattamento definitivo
Giacomo Germani - Encefalopatia: management clinico e prevenzione delle recidive
Il Prof. Germani ha iniziato la sua presentazione con la descrizione degli obiettivi del trattamento, specificando che il trattamento va riservato ai pazienti con encefalopatia conclamata perche il rapporto costo-benefico del trattamento della encefalopatia minima non è ancora così evidente.
Gli obiettivi del trattamento durante un episodio acuto di EE sono:
- migliorare lo stato neurologico
- identificare e trattare il fattore precipitante
- ridurre la durata dell’episodio
- limitarne le conseguenze
Dopo il primo episodio di EE conclamata, la terapia dovrebbe mirare a:
- prevenire le recidive e i ricoveri ospedalieri
- migliorare la qualità della vita
- ridurre l’impatto sulla famiglia del paziente
È necessario intervenire sui fattori predisponenti che sono stati già presentati e sicuramente l’intervento precoce su questi risulta fondamentale nella risoluzione di EE. I farmaci disponibili sono targetizzati secondo i meccanismi fisiopatologici della malattia e quindi il primo loro obiettivo è la riduzione dei livelli di ammonio nel torrente ematico, favorendo il ciclo dell’aurea a livello epatico. Importante appare anche la modulazione del microbiota intestinale.
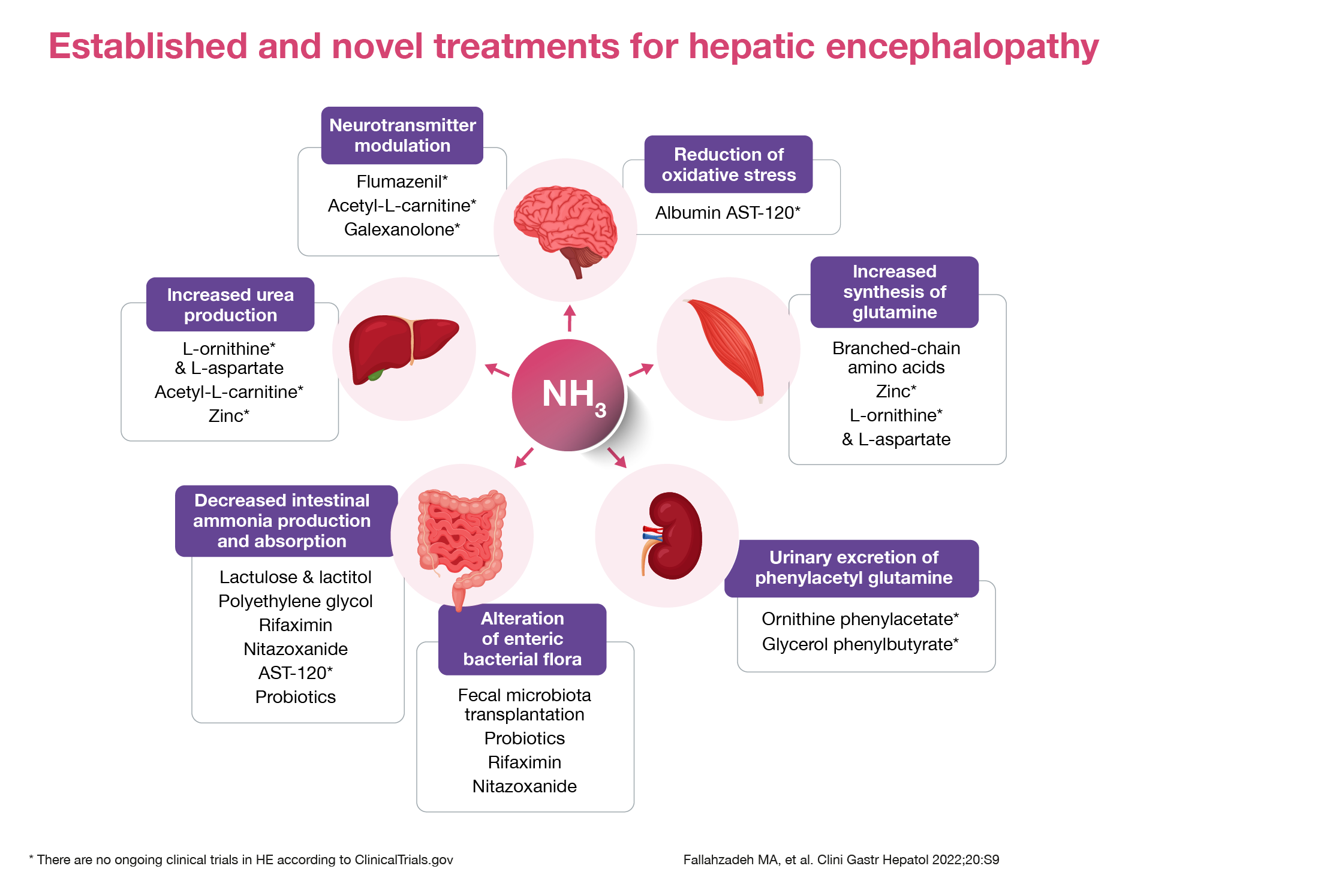
I farmaci maggiormente utilizzati nella terapia dell’EE, sono:
- disaccardi non assorbibili, tra cui il lattulosio, il farmaco più utilizzato
- rifaximina (antibiotico ad ampio spettro) ha dimostrato una significativa efficacia nella riduzione di nuovi episodi di EE nei pazienti con un episodio di EE precedente.

Lascia un commento